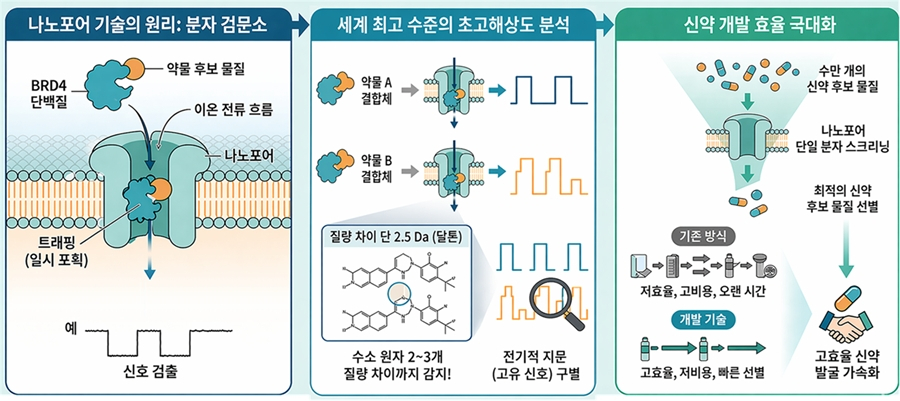
이 기술은 기존에 구분이 거의 불가능했던 미세한 질량 차이까지 식별할 수 있어 차세대 신약개발 속도를 크게 높일 것으로 기대된다.
한국생명공학연구원(이하 생명연) AI바이오의약연구소 지승욱·정기백·황성보·김진식 박사 공동연구팀은 단백질-약물 결합 상태를 단일분자 수준에서 분석할 수 있는 초정밀 나노포어(nanopore) 센서를 개발했다.
나노포어는 분자가 지나갈 때 발생하는 미세한 전류 변화를 읽어 생체분자 특성을 분석하는 초미세 구멍 기반 센서 기술이다.
단백질이 나노포어 구멍을 통과하거나 내부에 머무르면 전류 흐름이 미세하게 변하고, 이 신호를 정밀 분석해 단백질과 약물의 결합 상태를 판별할 수 있다.
신약 개발은 수많은 후보 물질 가운데 특정 단백질에 정확히 결합하는 약물을 선별하는 과정이 핵심이다.
하지만 구조가 매우 비슷한 저분자 약물은 단백질과 결합했을 때 차이가 극히 미세해 기존 기술로는 정확한 분석이 쉽지 않았다.
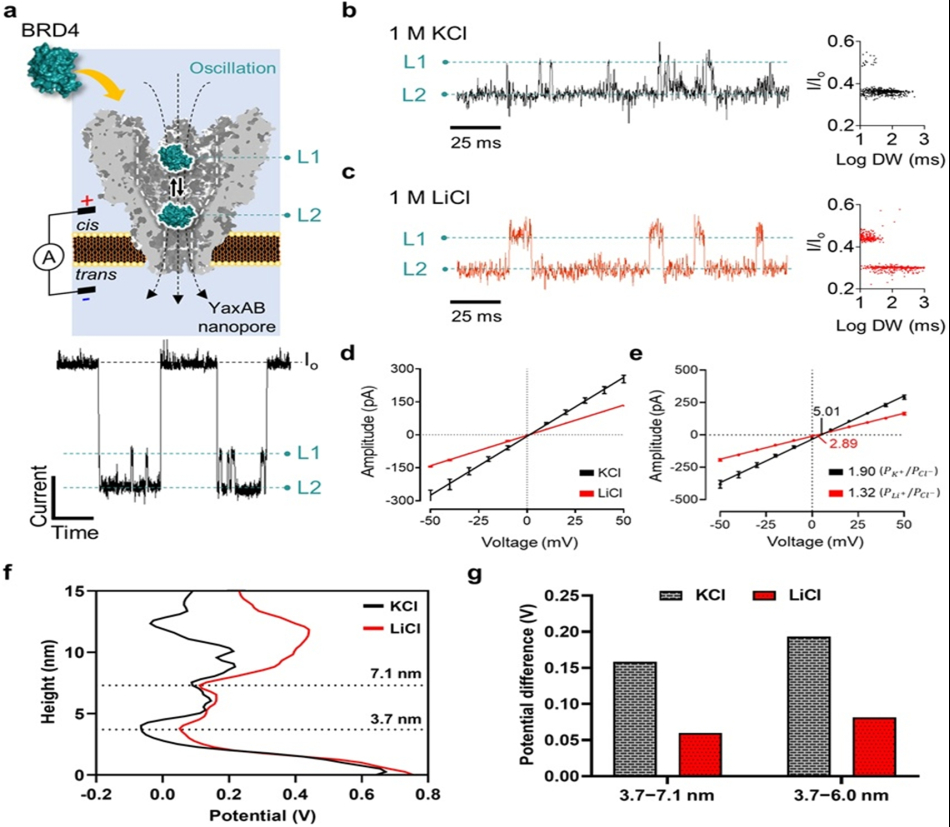
연구팀은 예르시니아 엔테로콜리티카 박테리아 독소 단백질에서 유래한 ‘YaxAB 나노포어’를 센서로 사용했다.
이 나노포어는 입구는 넓고 출구는 좁은 깔때기 형태 구조로, 내부에서 강한 전기삼투 흐름을 만들어 단백질을 안정적으로 가둘 수 있는 특징이 있다.
연구팀은 항암제 개발의 핵심 표적으로 꼽히는 BRD4 단백질을 대상으로 실험한 진행했다.
BRD4는 유전자 발현과 DNA 복제를 조절하는 단백질로, 다양한 항암 신약 개발이 진행 중인 주요 표적이다.
연구팀은 약물 종류에 따라 서로 다른 전기 신호 패턴을 분석해 질량 차이가 2.5Da(달톤)에 불과한 약물까지 구별하는 데 성공했다.
이는 수소 원자 2~3개 정도 차이에 해당하는 수준이다.
기존 나노포어 기반 단백질 분석은 대체로 88~116달톤 수준 차이를 구분하는 데 머물렀다.
이번 연구는 그보다 수십 배 높은 해상도를 구현한 것으로, 자연 상태 단백질 분석 분야에서 세계 최고 수준이다.
이를 통해 단백질이 나노포어 내부 어느 위치에 머무는지, 얼마나 진동하는지, 전류 노이즈가 어떻게 변하는지를 함께 분석해 약물별 고유한 ‘전기적 지문’을 확보했다.
특히 전류 신호를 40㎳ 단위로 세분화해 노이즈 특성을 분석하는 새로운 방법을 적용했다.
이 방법은 기존 표준편차 기반 분석보다 훨씬 높은 78.6% 수준의 분별 성능을 보였다.
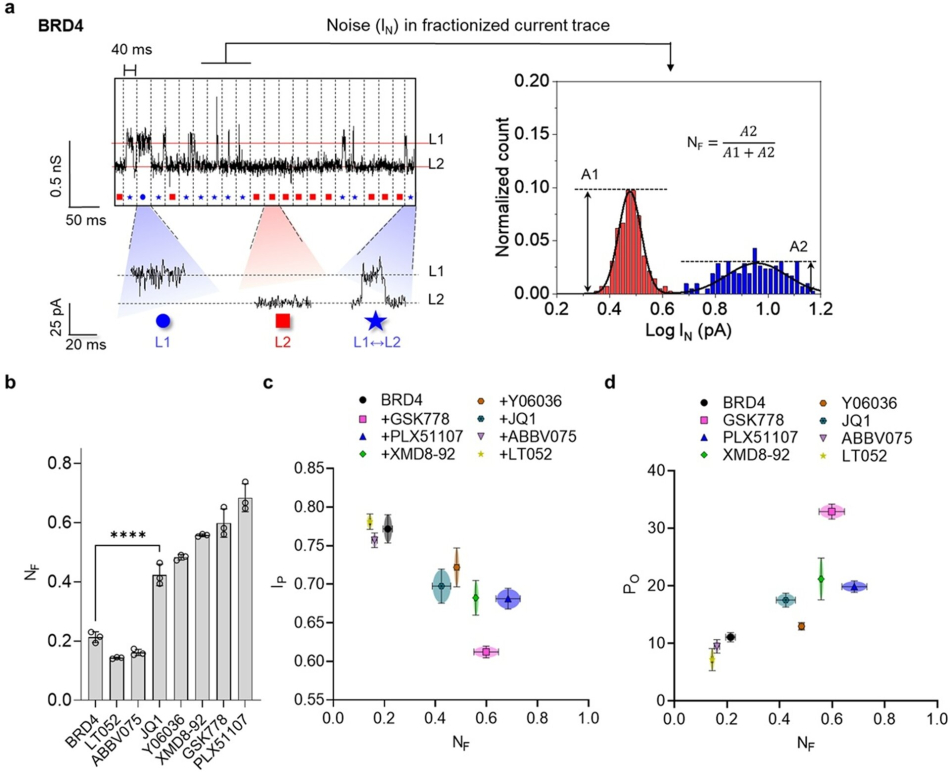
또 구조가 유사한 약물들의 미세한 결합 차이를 정밀하게 분석할 수 있어 약물 구조와 효능 관계를 분석하는 ‘구조-활성 관계(SAR)’ 연구에도 적용할 수 있어 차세대 신약 스크리닝 기술로 발전시킬 수 있을 것으로 기대받고 있다.
지 박사는 “이번 연구는 원자 수준에서 단백질-약물 결합을 분석할 수 있는 세계 최고 수준의 고해상도 나노포어 센서 기술”이라며 “고효율 신약 발굴뿐 아니라 정밀의료와 질병 진단 플랫폼으로도 확장 가능성이 크다”고 설명했다.
한편, 이번 연구는 생명연 김진식 박사와 조준혁 UST-생명연 스쿨 박사과정이 제1저자로 수행했고, 연구결과는 지난달 27일 국제학술지 ‘ACS Nano(IF 16.1)’ 온라인에 게재됐다.
(논문명: Nanopore Discrimination of Protein–Small-molecule Drug Complexes at Near-Atomic Resolution)