
신약 허가·심사 속도를 높이기 위한 정부의 규제 개편이 본궤도에 올랐다. 식품의약품안전처는 최근 허가·심사 지원 인력 195명을 새로 임용하고, 오는 10월부터 240일 심사 체계를 적용할 방침이다. 다만 제약바이오 업계에선 인력 유출과 졸속 심사에 따른 의약품 안전성 우려, 수수료 인상 부담 등을 지적하는 목소리도 적지 않다.
21일 업계에 따르면 정부는 신약 허가 신청부터 최종 심사까지 걸리는 기간을 240일로 줄이기 위한 채비를 서두르고 있다. 심사 인력 대폭 확충과 병렬 심사 체계 도입으로 환자의 치료 기회를 앞당기겠다는 구상이다. 희귀질환 치료제의 건강보험 등재 기간은 100일 이내로 줄이며, 중증·난치질환 치료제 등 혁신 신약의 가치를 평가·조정하는 비용효과성 평가 체계도 단계적으로 고도화한다.
이를 위해 식약처는 공무원 195명을 신규 임용했다. 일반직 공무원 19명(약무 15명, 의료기술 4명), 연구직 공무원 176명(보건연구 125명, 공업연구 51명)이다. 이번 채용에 약 2400명이 지원해 12대 1의 경쟁률을 보였다. 신규 임용자는 △신약·희귀의약품 등의 품질심사 △바이오시밀러(바이오의약품 복제약)의 품질과 안전·유효성 평가 △인공지능(AI) 등 신기술 의료기기의 안전·유효성 검증 등 핵심 분야에 배치된다.
이번 인력 확충은 지난해 10월16일 이재명 대통령 주재 ‘제2차 핵심규제 합리화 전략회의’에서 논의된 바이오헬스 핵심 규제 합리화 정책의 일환이다. 당시 이 대통령은 바이오산업에서 실증과 임상, 치료가 빠르게 이루어지도록 제도 개편을 주문하며 “전통적인 규제 담당 기관들도 해당 분야의 성장과 진흥에 대한 책임을 다해야만 민간 부문의 무한한 창의성과 반 발짝 앞선 속도를 뒷받침할 수 있다”고 말했다.
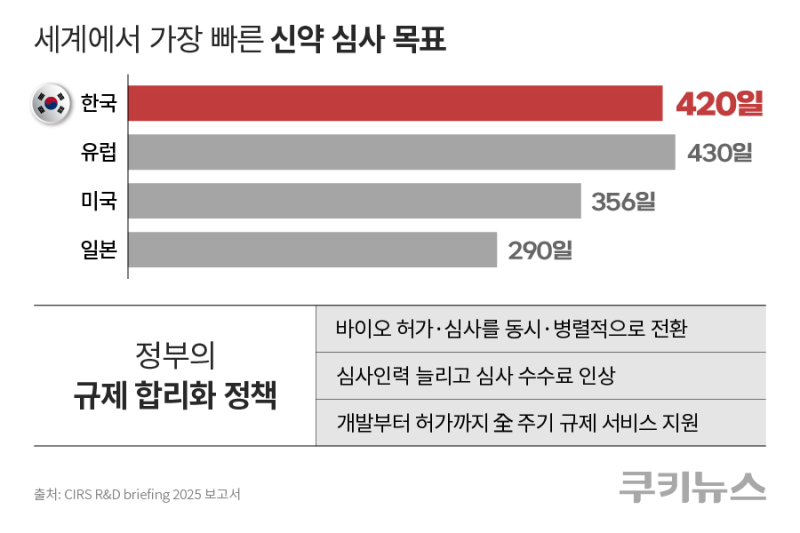
韓 신약 심사 기간 420일…日 290일
정부가 ‘세계 최단’ 허가·심사 속도를 내걸은 이유는 국내 신약 심사에 소요되는 기간이 해외 주요국보다 월등히 길기 때문이다. 글로벌 규제 컨설팅 전문기업 CIRS 그룹이 내놓은 ‘연구개발(R&D) 브리핑 2025’ 보고서에 따르면, 한국의 신약 심사 기간은 420일에 달한다. 일본 290일, 미국 356일과 비교해 긴 편이며, 유럽(430일)과 비슷한 수준이다. 국내에서 의료기기는 평균 398일 가량 소요된다.
식약처 심사 인력도 다른 국가에 비해 현저히 적다. 지난해 10월 식약처가 남인순 더불어민주당 의원실에 제출한 ‘주요국 심사 인력 현황 및 신약 허가’ 자료에 따르면, 국내 심사 인력은 369명에 불과했다. 이는 미국 식품의약국(FDA) 9049명, 유럽 의약품청(EMA) 4000명, 일본 의약품의료기기종합기구(PMDA) 635명에 비해 적은 수준이다. 심사 1건당 투입 인력도 식약처는 3~5명이지만, 미국 FDA는 40명, 유럽 EMA는 20명, 일본 PMDA는 15명에 달한다.
국내 신약 심사 규제 개선이 지지부진한 사이 중국은 지속적인 정부 투자와 국제 기준에 부합하는 규제 체계 개편, 전문 인력 확충 등으로 글로벌 신약 시장에서 경쟁력을 확보했다. 중국 정부는 지난 2016년 ‘건강중국 2030’ 계획을 발표하며 헬스케어 투자 규모를 오는 2030년 16조위안(약 3000조원)까지 늘리겠다는 계획을 내놨다. 지난해 바이오산업에 투입한 자금은 300억위안(약 5조8000억원)에 달한다. 임상시험 신청 심사 기한은 일부 조건 하에 30일로 줄이고, 수익성 없는 기술 스타트업의 상장을 지원하기 위한 상장 제도도 개편했다.
이에 정부는 심사 인력을 300명 확대할 계획이다. 대신 소요되는 150억원의 예산을 신약 심사 비용 증액으로 충당한다. 식약처는 신약 심사료(허가 수수료)를 기존 803만원에서 바이오시밀러는 3억1000만원, 신약은 4억1000만원으로 각각 올리기로 했다.
기대·우려 교차…“수수료 인상·인력 유출 걱정”
정부의 정책 방향을 두고 업계에선 기대와 우려가 교차한다. 글로벌 제약사 A관계자는 “현재로선 지금의 변화가 심사비를 더 받기 위한 명분처럼 보인다”며 “허가나 급여 절차가 얼마나 빨라질지에 대해선 현장의 체감이 거의 없다는 의견도 많다”고 말했다. 제도가 바뀌더라도 실제 환자나 업계가 느끼는 변화가 없다면 설득력이 떨어질 수밖에 없다는 지적이다.
다른 글로벌 제약사 B관계자는 “정부가 심사비로 4억원을 받겠다고 하면 그 돈을 어디에 어떻게 쓸 것인지에 대한 구체적인 설명이 있어야 한다”며 “신약 허가와 급여는 별개 절차이기 때문에 앞으로 어떤 방식으로 제도가 운영되는지 명확히 볼 필요가 있다”고 짚었다.

의약품의 충분한 검토 없이 속도만 앞세울 경우 졸속 심사로 이어질 수 있다는 우려도 나온다. B관계자는 “신약은 무엇보다 안전성과 유효성 검증이 핵심인 만큼, 인력 확충만으로 심사 품질까지 단기간에 확보할 수 있을지는 지켜봐야 한다”면서 “환자의 치료 접근성을 높이는 것도 중요하지만, 의약품 안전성에 대한 신뢰가 흔들려선 안 된다”고 강조했다.
인력 유출에 대한 걱정도 있다. 글로벌 제약사 C관계자는 “심사 인력을 대거 충원하며 글로벌 제약사 등 민간 영역의 전문 인력이 일부 유출될 가능성이 있다”며 “실제 관련 인력을 상당수 채용한 것으로 알고 있다”고 전했다.
신규 임용된 심사 인력들은 현장 투입에 앞서 3주간의 직무교육과 함께 의약품 품질·안전성·유효성 심사, 의료기기 성능 심사 및 안전관리 등 분야별 전문교육을 받게 된다. 식약처는 신규 임용자들이 단기간에 실무 전문성을 확보하고, 교육 이후 심사·평가 현장에 즉시 투입될 수 있도록 분야별 관련 법령, 국제 가이드라인, 최신 규제 동향 등과 함께 실제 허가·심사 사례에 대한 실무 중심의 교육을 제공할 예정이다.
오유경 식약처장은 “앞으로도 허가·심사와 규제 혁신을 통해 변화하는 글로벌 바이오헬스 환경에 선제적으로 대응하고, 국민건강 보호와 산업 발전을 동시에 달성할 수 있도록 지속적으로 노력하겠다”고 밝혔다.



